祥符实验室赵磊博士与上海交通大学合作团队发展了一种支持通用性数字计算的DNA可编程门阵列(DNA-based programmable gate array, DPGA),可通过分子指令编程的方式实现通用数字DNA计算,实现了无衰减大规模液相分子电路的构建。该成果近期发表于《自然》(Nature)杂志。
1994年,图灵奖得主Adleman提出利用DNA的碱基互补配对原则来发展生物计算。自那以后,基于DNA分子间相互作用的液相DNA分子计算,已在高并行编码与执行算法方面展现出巨大的潜能。此前,研究者利用DNA分子反应网络,成功实现了细胞自动机、逻辑电路、决策机器、神经网络等多种功能。然而,现有的DNA计算体系仅能针对特定功能进行硬件定制。而在电子计算机领域,通用性集成电路(如FPGA)可通过软件编程的方式执行各种运算功能,而无需从头设计制造硬件,这为研发计算机器提供了高阶平台。因此,如何发展具有通用性的DNA运算元件的编程与集成已成为制约DNA计算领域发展的瓶颈。
针对这一挑战性问题,研究团队首先证明了利用单链DNA作为统一传输信号(DNA-UTS),可实现类似电子在电路中传输的功能。进而,开发了一种支持通用性数字计算的DPGA,并支持器件层次的多DPGA集成,实现了器件内的可编程性和器件间可集成性。(图1)。如,当电路的复杂度超出单个DPGA可执行规模时,DPGA可分解为多个子任务,并生成对应的分子指令;每一个子电路的分子指令通过逻辑地址调用并连接参与运算的DNA元件,实现DPGA的编程;子电路之间的信号传输则通过DNA折纸寄存器介导的多DPGA布线实现,从而实现器件级的多DPGA集成。
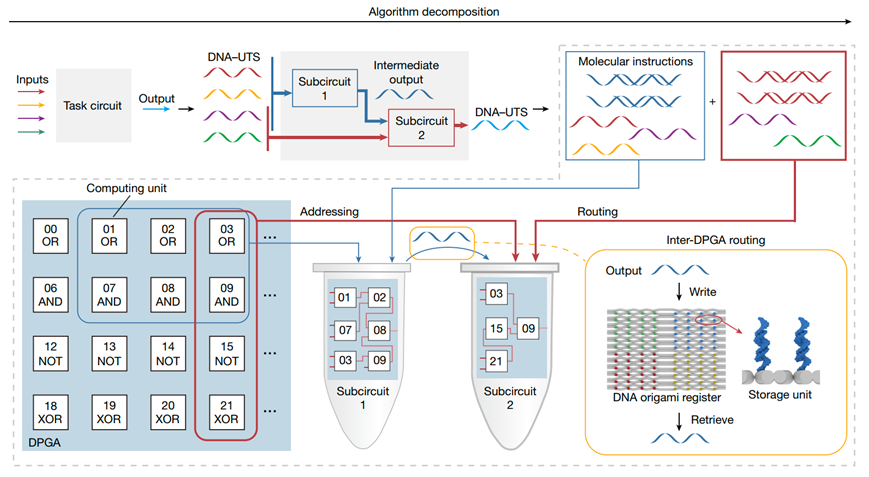
图1
利用DPGA的可编程性与高集成度,本研究突破了DNA分子计算在电路规模和电路深度的瓶颈,首次在实验上展示了高达30个逻辑元件、500条DNA链,包含30层DNA链取代反应的电路规模。这也代表了近20年来DNA计算领域的新突破(图2)。
进一步的研究发现DNA-UTS在跨越多个DPGA传输的过程中没有显著衰减,证明了DPGA的高度可扩展性。这预示着任何实际问题,理论上都可以在模数转换后,通过DNA-UTS接入DPGA电路。本研究中概念性展示了将DPGA作为为分子诊断中的信息处理核心,对疾病相关的分子靶标进行非线性分类。
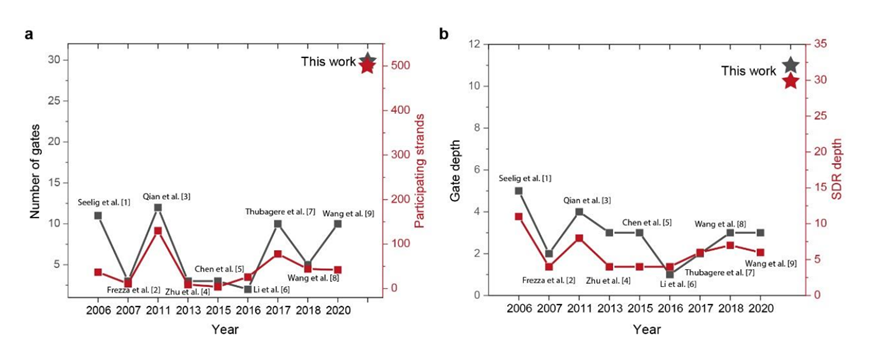
图2
本论文由上海交通大学樊春海院士团队领衔、祥符实验室参与并共同完成。
论文链接:https://doi.org/10.1038/s41586-023-06484-9
